摘要:新研究表明,在嬰兒時(shí)期的關(guān)鍵發(fā)育窗口期接觸抗生素會(huì)阻礙胰腺中產(chǎn)生胰島素的細(xì)胞的生長。
一項(xiàng)針對(duì)小鼠的新研究表明,在嬰兒時(shí)期的關(guān)鍵發(fā)育窗口期接觸抗生素會(huì)阻礙胰腺中產(chǎn)生胰島素的細(xì)胞的生長,并可能增加以后患糖尿病的風(fēng)險(xiǎn)。
本月發(fā)表在《科學(xué)》(Science)雜志上的這項(xiàng)研究還指出了可能有助于這些關(guān)鍵細(xì)胞在生命早期增殖的特定微生物。
 圖1 真菌促進(jìn)新生兒β細(xì)胞發(fā)育與代謝健康
圖1 真菌促進(jìn)新生兒β細(xì)胞發(fā)育與代謝健康這一發(fā)現(xiàn)是揭示人類嬰兒微生物群重要性的最新發(fā)現(xiàn)。嬰兒微生物群是指在我們最初幾年里生活在我們身上和體內(nèi)的細(xì)菌和真菌群。這項(xiàng)研究可能會(huì)為解決一系列代謝疾病帶來新的方法。
科羅拉多大學(xué)生物前沿研究所分子、細(xì)胞和發(fā)育生物學(xué)助理教授、第一作者詹妮弗·希爾說:“我們希望我們的研究能讓人們更多地認(rèn)識(shí)到嬰兒微生物群對(duì)發(fā)育的重要性。這項(xiàng)工作也提供了重要的新證據(jù),表明基于微生物的方法有一天不僅可以用來預(yù)防糖尿病,還可以用來逆轉(zhuǎn)糖尿病。”
環(huán)境中的某些東西
超過200萬美國成年人患有1型糖尿病,這是一種無法治愈的疾病,患者的胰腺無法分泌胰島素(將葡萄糖轉(zhuǎn)化為能量的激素),血液中充滿了糖分。
這種疾病通常出現(xiàn)在兒童時(shí)期,遺傳因素在其中起著重要作用。但科學(xué)家們發(fā)現(xiàn),雖然同卵雙胞胎的DNA相同,使他們?nèi)菀谆?型糖尿病,但通常只有一對(duì)雙胞胎會(huì)患這種疾病。
希爾說:“這告訴你,它們的環(huán)境經(jīng)歷正在改變它們的易感性。”
多年來,她一直在尋找微生物的答案。
先前的研究表明,母乳喂養(yǎng)或順產(chǎn)出生的孩子比其他孩子患1型糖尿病的可能性更小,這兩種方式都能促進(jìn)健康的嬰兒微生物群。一些研究還表明,早期給嬰兒服用抗生素可能會(huì)無意中殺死有益細(xì)菌和有害細(xì)菌,并增加患糖尿病的風(fēng)險(xiǎn)。
揮之不去的問題是:這些嬰兒錯(cuò)過了哪些微生物?
希爾說:“我們的研究發(fā)現(xiàn),在生命早期,特定的微生物是促進(jìn)胰腺細(xì)胞發(fā)育所必需的,這是一個(gè)關(guān)鍵的窗口。”
一個(gè)關(guān)鍵的機(jī)會(huì)窗口
她解釋說,人類嬰兒出生時(shí)只有少量的胰腺“β細(xì)胞”,這是體內(nèi)唯一能產(chǎn)生胰島素的細(xì)胞。
但在嬰兒一歲的某個(gè)時(shí)候,β細(xì)胞生長出現(xiàn)了一生一次的激增。
希爾說:“無論出于何種原因,如果我們沒有經(jīng)歷這種擴(kuò)張和增殖,這可能是糖尿病的原因。”
她是猶他大學(xué)的博士后研究員,與資深作者、病理學(xué)教授瓊·朗德(June Round)一起進(jìn)行了這項(xiàng)研究。
他們發(fā)現(xiàn),當(dāng)他們?cè)谝粋€(gè)特定的窗口期(相當(dāng)于人類大約7到12個(gè)月的壽命)給小鼠服用廣譜抗生素時(shí),小鼠的胰島素產(chǎn)生細(xì)胞減少,血糖水平升高,胰島素水平降低,成年后代謝功能普遍變差。
“對(duì)我來說,這太令人震驚了,有點(diǎn)嚇人。”“這表明微生物群在這個(gè)非常短的早期發(fā)育時(shí)期是多么重要。”
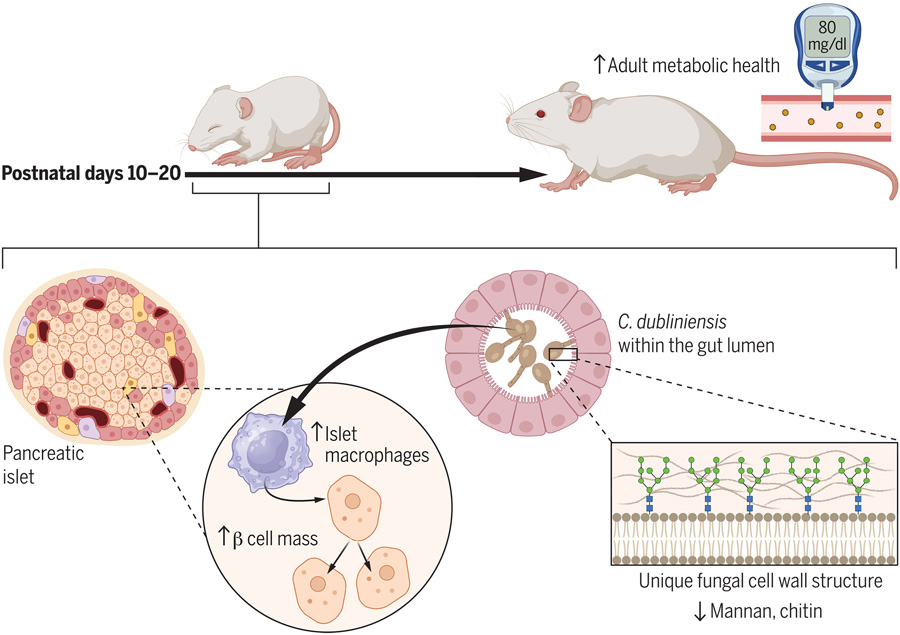
圖2 都柏林念珠菌定植促進(jìn)出生后胰腺發(fā)育
嬰兒便便的教訓(xùn)
在其他實(shí)驗(yàn)中,科學(xué)家們給小鼠注射了特定的微生物,發(fā)現(xiàn)其中一些微生物增加了它們的β細(xì)胞的產(chǎn)生,提高了血液中的胰島素水平。
其中最強(qiáng)大的是一種叫做都柏林念珠菌的真菌。
研究小組使用了“青少年糖尿病的環(huán)境決定因素”(TEDDY)研究中的糞便樣本,制作了希爾所說的“糞便冰沙”,并喂給小鼠。
當(dāng)研究人員用7到12個(gè)月大的健康嬰兒的糞便接種新生小鼠時(shí),它們的β細(xì)胞開始生長。其他年齡段嬰兒的糞便則沒有同樣的效果。
值得注意的是,只有在這一時(shí)期,都柏林假絲酵母在人類嬰兒中才大量存在。
希爾說:“這表明人類也有一個(gè)被這些促進(jìn)細(xì)胞的微生物定植的狹窄窗口。”
當(dāng)遺傳上易患1型糖尿病的雄性小鼠在嬰兒期被真菌定植時(shí),它們患糖尿病的幾率不到15%。沒有接受真菌的雄鼠有90%的幾率得糖尿病。
更有希望的是,當(dāng)研究人員將這種真菌注射到產(chǎn)生胰島素的細(xì)胞被殺死的成年小鼠身上時(shí),這些細(xì)胞又再生了。
治療為時(shí)過早
希爾強(qiáng)調(diào),她不是“反抗生素者”。
但她確實(shí)想象有一天,醫(yī)生可以在使用抗生素的同時(shí),給病人服用基于微生物的藥物或補(bǔ)充劑,以取代無意中殺死的促進(jìn)新陳代謝的細(xì)菌。
糞便冰沙(糞便微生物群移植)已經(jīng)被實(shí)驗(yàn)用于改善2型糖尿病患者的代謝狀況,2型糖尿病也會(huì)損害胰腺細(xì)胞。
但這種方法可能會(huì)帶來真正的風(fēng)險(xiǎn),因?yàn)樵S多對(duì)兒童有益的微生物可能會(huì)對(duì)成年人造成傷害。相反,她希望科學(xué)家有一天能夠利用微生物的特定機(jī)制來開發(fā)新的治療方法,以治療受損的胰腺逆轉(zhuǎn)糖尿病。
她最近幫助在科羅拉多大學(xué)博爾德分校建立了一個(gè)最先進(jìn)的“無菌”設(shè)施,用于研究嬰兒微生物群。在那里,動(dòng)物可以在完全沒有微生物的無菌“氣泡”中繁殖和飼養(yǎng),通過一個(gè)接一個(gè)地重新引入它們,科學(xué)家可以了解它們是否有效。
“從歷史上看,我們一直認(rèn)為細(xì)菌是我們想要避免的東西,但我們可能有比病原體更多的有益微生物,”她說。“通過利用它們的力量,我們可以為人類健康做很多事情。”
參考資料
[1] Neonatal fungi promote lifelong metabolic health through macrophage-dependent β cell development
摘要:新研究表明,在嬰兒時(shí)期的關(guān)鍵發(fā)育窗口期接觸抗生素會(huì)阻礙胰腺中產(chǎn)生胰島素的細(xì)胞的生長。
一項(xiàng)針對(duì)小鼠的新研究表明,在嬰兒時(shí)期的關(guān)鍵發(fā)育窗口期接觸抗生素會(huì)阻礙胰腺中產(chǎn)生胰島素的細(xì)胞的生長,并可能增加以后患糖尿病的風(fēng)險(xiǎn)。
本月發(fā)表在《科學(xué)》(Science)雜志上的這項(xiàng)研究還指出了可能有助于這些關(guān)鍵細(xì)胞在生命早期增殖的特定微生物。
 圖1 真菌促進(jìn)新生兒β細(xì)胞發(fā)育與代謝健康
圖1 真菌促進(jìn)新生兒β細(xì)胞發(fā)育與代謝健康這一發(fā)現(xiàn)是揭示人類嬰兒微生物群重要性的最新發(fā)現(xiàn)。嬰兒微生物群是指在我們最初幾年里生活在我們身上和體內(nèi)的細(xì)菌和真菌群。這項(xiàng)研究可能會(huì)為解決一系列代謝疾病帶來新的方法。
科羅拉多大學(xué)生物前沿研究所分子、細(xì)胞和發(fā)育生物學(xué)助理教授、第一作者詹妮弗·希爾說:“我們希望我們的研究能讓人們更多地認(rèn)識(shí)到嬰兒微生物群對(duì)發(fā)育的重要性。這項(xiàng)工作也提供了重要的新證據(jù),表明基于微生物的方法有一天不僅可以用來預(yù)防糖尿病,還可以用來逆轉(zhuǎn)糖尿病。”
環(huán)境中的某些東西
超過200萬美國成年人患有1型糖尿病,這是一種無法治愈的疾病,患者的胰腺無法分泌胰島素(將葡萄糖轉(zhuǎn)化為能量的激素),血液中充滿了糖分。
這種疾病通常出現(xiàn)在兒童時(shí)期,遺傳因素在其中起著重要作用。但科學(xué)家們發(fā)現(xiàn),雖然同卵雙胞胎的DNA相同,使他們?nèi)菀谆?型糖尿病,但通常只有一對(duì)雙胞胎會(huì)患這種疾病。
希爾說:“這告訴你,它們的環(huán)境經(jīng)歷正在改變它們的易感性。”
多年來,她一直在尋找微生物的答案。
先前的研究表明,母乳喂養(yǎng)或順產(chǎn)出生的孩子比其他孩子患1型糖尿病的可能性更小,這兩種方式都能促進(jìn)健康的嬰兒微生物群。一些研究還表明,早期給嬰兒服用抗生素可能會(huì)無意中殺死有益細(xì)菌和有害細(xì)菌,并增加患糖尿病的風(fēng)險(xiǎn)。
揮之不去的問題是:這些嬰兒錯(cuò)過了哪些微生物?
希爾說:“我們的研究發(fā)現(xiàn),在生命早期,特定的微生物是促進(jìn)胰腺細(xì)胞發(fā)育所必需的,這是一個(gè)關(guān)鍵的窗口。”
一個(gè)關(guān)鍵的機(jī)會(huì)窗口
她解釋說,人類嬰兒出生時(shí)只有少量的胰腺“β細(xì)胞”,這是體內(nèi)唯一能產(chǎn)生胰島素的細(xì)胞。
但在嬰兒一歲的某個(gè)時(shí)候,β細(xì)胞生長出現(xiàn)了一生一次的激增。
希爾說:“無論出于何種原因,如果我們沒有經(jīng)歷這種擴(kuò)張和增殖,這可能是糖尿病的原因。”
她是猶他大學(xué)的博士后研究員,與資深作者、病理學(xué)教授瓊·朗德(June Round)一起進(jìn)行了這項(xiàng)研究。
他們發(fā)現(xiàn),當(dāng)他們?cè)谝粋€(gè)特定的窗口期(相當(dāng)于人類大約7到12個(gè)月的壽命)給小鼠服用廣譜抗生素時(shí),小鼠的胰島素產(chǎn)生細(xì)胞減少,血糖水平升高,胰島素水平降低,成年后代謝功能普遍變差。
“對(duì)我來說,這太令人震驚了,有點(diǎn)嚇人。”“這表明微生物群在這個(gè)非常短的早期發(fā)育時(shí)期是多么重要。”

圖2 都柏林念珠菌定植促進(jìn)出生后胰腺發(fā)育
嬰兒便便的教訓(xùn)
在其他實(shí)驗(yàn)中,科學(xué)家們給小鼠注射了特定的微生物,發(fā)現(xiàn)其中一些微生物增加了它們的β細(xì)胞的產(chǎn)生,提高了血液中的胰島素水平。
其中最強(qiáng)大的是一種叫做都柏林念珠菌的真菌。
研究小組使用了“青少年糖尿病的環(huán)境決定因素”(TEDDY)研究中的糞便樣本,制作了希爾所說的“糞便冰沙”,并喂給小鼠。
當(dāng)研究人員用7到12個(gè)月大的健康嬰兒的糞便接種新生小鼠時(shí),它們的β細(xì)胞開始生長。其他年齡段嬰兒的糞便則沒有同樣的效果。
值得注意的是,只有在這一時(shí)期,都柏林假絲酵母在人類嬰兒中才大量存在。
希爾說:“這表明人類也有一個(gè)被這些促進(jìn)細(xì)胞的微生物定植的狹窄窗口。”
當(dāng)遺傳上易患1型糖尿病的雄性小鼠在嬰兒期被真菌定植時(shí),它們患糖尿病的幾率不到15%。沒有接受真菌的雄鼠有90%的幾率得糖尿病。
更有希望的是,當(dāng)研究人員將這種真菌注射到產(chǎn)生胰島素的細(xì)胞被殺死的成年小鼠身上時(shí),這些細(xì)胞又再生了。
治療為時(shí)過早
希爾強(qiáng)調(diào),她不是“反抗生素者”。
但她確實(shí)想象有一天,醫(yī)生可以在使用抗生素的同時(shí),給病人服用基于微生物的藥物或補(bǔ)充劑,以取代無意中殺死的促進(jìn)新陳代謝的細(xì)菌。
糞便冰沙(糞便微生物群移植)已經(jīng)被實(shí)驗(yàn)用于改善2型糖尿病患者的代謝狀況,2型糖尿病也會(huì)損害胰腺細(xì)胞。
但這種方法可能會(huì)帶來真正的風(fēng)險(xiǎn),因?yàn)樵S多對(duì)兒童有益的微生物可能會(huì)對(duì)成年人造成傷害。相反,她希望科學(xué)家有一天能夠利用微生物的特定機(jī)制來開發(fā)新的治療方法,以治療受損的胰腺逆轉(zhuǎn)糖尿病。
她最近幫助在科羅拉多大學(xué)博爾德分校建立了一個(gè)最先進(jìn)的“無菌”設(shè)施,用于研究嬰兒微生物群。在那里,動(dòng)物可以在完全沒有微生物的無菌“氣泡”中繁殖和飼養(yǎng),通過一個(gè)接一個(gè)地重新引入它們,科學(xué)家可以了解它們是否有效。
“從歷史上看,我們一直認(rèn)為細(xì)菌是我們想要避免的東西,但我們可能有比病原體更多的有益微生物,”她說。“通過利用它們的力量,我們可以為人類健康做很多事情。”
參考資料
[1] Neonatal fungi promote lifelong metabolic health through macrophage-dependent β cell development



